Dell'elemento
Dal latino elementum, un elemento è un principio chimico o fisico questo fa parte della composizione di un Corposo. Per la filosofia antica, c'erano quattro elementi che erano i principi fondamentali che mediavano la costituzione degli organismi: aria, acqua, terra e fuoco.
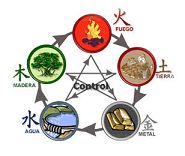
L'esistenza di questi quattro elementi essenziali fu postulata dai greci. Per i cinesi, invece, gli elementi erano cinque: acqua, terra, fuoco, legno e metallo. Vale la pena ricordare che la filosofia tradizionale cinese li intende come tipi di potere in costante interazione.
In altri modi, è visto come parte integrante di qualcosa, ma il pezzo che compone una struttura e i componenti di un gruppo umano. Per esempio: "La CPU è l'elemento centrale di un computer", "La mia squadra di lavoro è composta da quattro elementi fondamentali: il martello, la guida di caccia, i ragazzi e i vizi", "La polizia ha portato via le azioni degli elementi sovversivi dentro l'università pubblica".
Un elemento è, invece, un individuo che viene valutato positivamente o negativamente per lo sviluppo di un'azione comune: "Gómez è uno degli elementi più importanti nel gioco della nostra squadra", "Quest'uomo è un elemento molto importante che causa sempre problemi in ufficio".
Un elemento chimico da solo è definito come una sostanza che non può essere decomposta in una più semplice mediante una reazione chimica. Il termine si riferisce invece alla classe di atomi che hanno lo stesso numero di protoni nel loro nucleo.
Nel campo della chimica, esiste un modello di organizzazione degli elementi conosciuti chiamato tavola periodica; ne contiene più di 118, disposti secondo il loro peso atomico. Per quanto riguarda l'origine di qualsiasi elemento chimico, alcuni si trovano in natura, come parti di sostanze semplici o composti, mentre altri sono sviluppati artificialmente con l'aiuto di un acceleratore di particelle o di un reattore atomico, nel qual caso sono così instabili che possono esistere solo per una piccola frazione di secondo.
Sebbene ci siano diversi modi di organizzare gli elementi chimici, la distinzione tra metalli e non metalli è fondamentale. Ci sono numerose differenze tra questi gruppi, sia nelle loro proprietà chimiche che fisiche, e alcune di queste sono descritte in dettaglio di seguito.
I metalli:
* hanno un basso potere di ionizzazione e il loro peso specifico è alto;
* da soli hanno da uno a tre elettroni al vostro ultimo livello energetico;
* tranne il mercurio, il gallio, il cesio e il francio, sono tutti solidi;
* appaiono molto luminosi;
* conducono molto bene il calore e l'elettricità;
* sono malleabili e duttili;
* quando perdono elettroni, si ossidano;
* solo un atomo forma la loro molecola e quando la loro struttura cristallina si unisce all'ossigeno genera ossidi, che formano acqua quando reagiscono con l'acqua;
* quelli di tipo alcalino mostrano più attività;
Non metalli:
* tendono a guadagnare elettroni;
* hanno un alto potenziale di ionizzazione e il loro peso lo specifico è basso;
* con poche eccezioni, hanno da quattro a sette elettroni nel loro ultimo livello di energia;
* Esistono nelle tre fasi fisiche di aggregazione;
* il suo aspetto non è lucido;
* le sue prestazioni nella conduzione di elettricità e calore sono molto scarse;
* non sono malleabili o duttili;
* Attraverso il guadagno degli elettroni, vengono ridotti;
* un minimo di due atomi compongono le loro molecole;
* quando si combinano con l'ossigeno, generano anidridi, che reagiscono con l'acqua per produrre ossidi;
* i più attenti sono l'ossigeno e gli alogeni;
* molti di loro hanno l'allotropia, una proprietà che permette a certi elementi di avere strutture chimiche diverse (l'ossigeno, per esempio, può essere presente come O2, ossigeno atmosferico, o come O3, ozono).
 Definizione
Definizione
