Orbitale molecolare
Il primo passo che faremo per conoscere il significato del termine orbitale molecolare è scoprire l'origine etimologica delle due parole che lo formano:
-Orbitale, in primo luogo, deriva dal latino. Più specificamente, possiamo affermare che è il risultato della somma di due componenti lessicali: la parola "orbita", che può essere tradotta come "percorso di moto circolare", e il suffisso "-al".
-Molecolare, in secondo luogo, viene anche dal latino. Nel suo caso, emana da "molecularis", che equivale a "relativo alla quantità minima di una sostanza". Questa parola latina si è formata combinando tre componenti lessicali: il sostantivo "moli", che significa "massa"; il suffisso "-culum", utilizzato per indicare un diminutivo; e il suffisso "-ar", che equivale a "relativo a".
Per comprendere l'idea di un orbitale molecolare, è necessario prima definire altri termini che sono indispensabili alla comprensione della nozione. Come punto di partenza, deve essere chiaro che un atomo è una particella che non può essere divisa con un metodo chimico.
Gli atomi presentano un nucleo che è circondato da elettroni: cioè, particelle elementari che hanno una carica elettrica negativa. Gli elettroni ruotano quindi intorno al nucleo atomico con movimenti ondulatori.
L'area intorno al nucleo dove c'è un'alta probabilità di trovare un elettrone è chiamata orbitale atomico. È uno spazio intorno al nucleo in cui è molto probabile che si trovino gli elettroni.
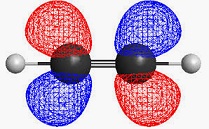
Ora possiamo concentrarci sulla definizione di orbitale molecolare. È la combinazione degli orbitali atomici di due atomi che sono legati insieme.
Un orbitale molecolare è formato da un insieme di orbitali atomici in un atomo di una molecola. La configurazione elettronica di ogni molecola dipende dai suoi orbitali molecolari.
Gli orbitali molecolari sono spesso legati a funzioni matematiche che riflettono il comportamento degli elettroni nelle molecole dal punto di vista della chimica quantistica. Le funzioni matematiche sono usate per descrivere il comportamento ondulatorio degli elettroni.
In altre parole, un orbitale molecolare è una regione spaziale che ha la densità elettronica indicata dalle funzioni matematiche. Queste funzioni, a loro volta, sono utilizzate per calcolare le proprietà fisiche e chimiche.
È importante menzionare che gli orbitali molecolari possono essere di legame (hanno meno energia degli orbitali atomici che permettono la loro creazione e sono in uno stato di attrazione) o anti-bonding (hanno più energia di ogni orbitale atomico e sono in uno stato di repulsione).
In aggiunta a quanto sopra, non possiamo trascurare il fatto che gli orbitali molecolari hanno la peculiarità di potersi caricare o riempire di elettroni in tre modi diversi. In particolare, per mezzo di questi:
- Per mezzo del principio di esclusione di Pauli. In questo passo, si indica che gli orbitali in questione possono ospitare un massimo di due elettroni quando vengono creati.
-Con un ordine chiaramente decrescente di livello energetico. In questo caso, si deve stabilire che gli orbitali molecolari di legame saranno caricati di elettroni prima di quelli di anti-legame.
- Attraverso la regola di Hund della massima duplicità. Questa è l'opzione che si prende quando l'obiettivo è quello di ottenere orbitali che rispondano al nome di orbitali semipieni.
 Definizione
Definizione
